Оксиды углерода и азота. Парниковый эффектМедицинская экология / Экологическая и эколого-медицинская характеристика атмосферы / Оксиды углерода и азота. Парниковый эффектСтраница 4
Оксиды азота. Помимо выбросов автотранспорта, в которых содержание оксидов азота (N0) может доходить до 1000 мг/мз, эти соединения попадают в атмосферу из природных источников:
• при грозовых разрядах и молниях;
• горении биомассы;
• денитрификации.
В качестве других антропогенных источников фигурирует производство красок и нитроцеллюлозы.
Для экологически благополучных районов естественная фоновая концентрация оксидов азота равна 0,08 мкг/м (Арктика), в средних широтах - 1,23 мкг/м что существенно ниже значения ПДК, равного 40 мкг/м
Оксиды азота техногенного происхождения образуются при сгорании топлива, если температура превышает 1000 °С. При высоких температурах часть молекулярного азота окисляется до оксида азота N0, который в воздухе немедленно вступает в реакцию с кислородом, образуя диоксид КОз и тетраоксид диазота N304. Первоначально образующийся оксид азота составляет лишь 10% выбросов всех оксидов азота в атмосферу, однако в воздухе значительная его часть превращается в диоксид - гораздо более опасное соединение.
Оксид азота (N0) - газ, не имеющий запаха. Его воздействие ведет к метгемоглобинообразованию, агрегации тромбоцитов и вазодилятации.
Диоксид азота (КОз) - газ с резким, раздражающим запахом, окрашенный в коричневый цвет (обонятельный порог 0,12 ррт). При контакте с влажной тканью легких образуется азотная кислота, что и ведет к патологии легких (тра-хеобронхиты, токсические пневмонии, вплоть до токсического отека легких). Патологии способствует повреждение диоксидом азота эластиновых и коллагеновых волокон соединительной ткани. Диоксид азота способен вызывать развитие аллергических реакций к другим веществам; усиливать восприимчивость к инфекционным заболеваниям легких, потенцировать бронхиальную астму и другие респираторные заболевания. Это особенно касается детей. Длительное воздействие высоких концентраций диоксида азота может приводить к хроническому воспалению ткани легких, которое по признакам напоминает эмфизему.
Добровольцы, получавшие ослабленный вирус гриппа наряду с воздействием диоксида азота, были более восприимчивы к вирусной инфекции, чем группа лиц, на которую не воздействовали диоксидом азота.
По данным ВОЗ при увеличении среднесуточной концентрации диоксида азота на 30 мкг/м число заболеваний нижних дыхательных путей у детей в возрасте 5—12 лет возрастает на 20%. В случае постоянного воздействия данного газа для расчета прироста частоты случаев заболеваний органов дыхания у детей в возрасте 6-7 лет используется уравнение 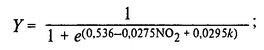
где Y— прирост числа случаев; NO2 — концентрация диоксида азота, мкг/мЗ; к — коэффициент: для мальчиков к = I, для девочек к = 0.
При увеличении среднесуточной концентрации диоксида азота на 10 мкг/м продолжительность приступов обострения заболеваний верхних дыхательных путей (в частности, бронхиальной астмы) возрастает на 6,5%.
Помимо этого, диоксид азота обладает способностью:,
• блокировать тиоловые группы ферментов, подавляя тканевое дыхание;
• снижать активность холинэстеразы;
• оказывать эмбрио- и гонадотоксическое действие;
• нарушать обмен витаминов группы С и В.
У растений диоксид азота нарушает фотосинтез и клеточный обмен.
Особенно опасную форму принимает загрязнение атмосферы оксидами азота при образовании так называемого фотохимического смога (англ. smoke дым + fog туман = smog).
Для его формирования необходимы следующие условия:
• температурная инверсия;
• солнечный свет;
• присутствие оксидов азота;
• наличие органических соединений в воздухе.
Температурная инверсия связана с застоем воздуха в силу тех обстоятельств, что слой теплого воздуха нависает над холодным приземным, задерживая конвекцию газов. Это
возможно после определенных метеоусловий, связанных с перемещением холодных воздушных масс. Особую важность приобретает рельеф местности, когда холодный воздух с возвышенности спускается в более низменную местность. При этом диоксид азота, поглощая УФИ Солнца, диссоциирует на оксид азота N0 и атомарный кислород О, который, соединяясь с молекулой О2, образует тропосферный озон - один из сильнейших окислителей. Наиболее благоприятное время для развития смога — с 10.00 до 16.00 ч в силу того, что в эти часы наиболее интенсивно УФИ (рис. 8.17).
Помимо этого, при одновременном присутствии в воздухе органических соединений типа углеводородов запускается цепь сложных химических реакций, в результате которых образуются альдегиды, кетоны, свободные радикалы, перок-сиды (например, пероксиацетилнитрат, являющийся сильным лакриматором). Вновь образованные вещества или фотохимические окислители по токсичности превосходят исходные продукты.
Смотрите также
Особенности природоохранной деятельности в России.
В нашей стране на первом этапе становления хозяйственного
механизма природопользования недостатки административной системы руководства
проявлялись более явно и отчетливо, чем в других странах. ...
Экономические методы охраны окружающей среды и особенности их использования в России
Проблема защиты экологии встала перед
человечеством сравнительно недавно. Но уже в нашем веке, который ознаменовал
себя масштабным истощением природных ресурсов, огромным количеством вредны ...
Структура сообщества
За исключением краткого рассмотрения биомов в гл. 3, до сих пор мы касались только
экологии особей и популяций. В этой главе речь пойдет об экологии сообществ. Подобно
тому как популяции обладают ...